CAR-T 细胞新突破:无细胞疗法能否改写癌症治疗规则?
发布时间:2025-08-21

近年来,癌症免疫治疗领域的明星——CAR-T 细胞疗法,以 “改造患者自身免疫细胞攻击癌细胞” 的创新机制,在白血病、淋巴瘤等血液肿瘤中展现了突破性疗效。然而,这种 治疗方法也面临着严峻挑战:可能引发严重的细胞因子释放综合征(发热、器官衰竭等)、对实体肿瘤渗透能力有限、制备成本高昂等。
有没有一种方法,既能保留 CAR-T 细胞的抗癌威力,又能规避这些风险?科学家将目光投向了细胞间通讯的 “纳米信使”——外泌体。最近一项发表在《Stem Cell Research & Therapy》的综述指出,CAR-T 细胞衍生的外泌体(简称 CAR-T 外泌体)可能成为下一代癌症治疗的关键突破点。
外泌体是细胞分泌的一种微小囊泡(直径约 30-150 纳米),就像细胞间的 “快递包裹”,内部携带蛋白质、RNA 等生物分子,负责在细胞间传递信号。几乎所有细胞都能分泌外泌体,其内容物反映了来源细胞的特性。例如,免疫细胞的外泌体可传递免疫信号,癌细胞的外泌体则可能帮助肿瘤逃避免疫攻击。
天然优势
①体积小:能穿透传统药物难以到达的组织(如实体肿瘤的致密基质);
②低免疫原性:作为 “无细胞” 载体,引发免疫反应的风险远低于活细胞;
③可修饰性:能通过基因工程加载特定靶向分子或药物。
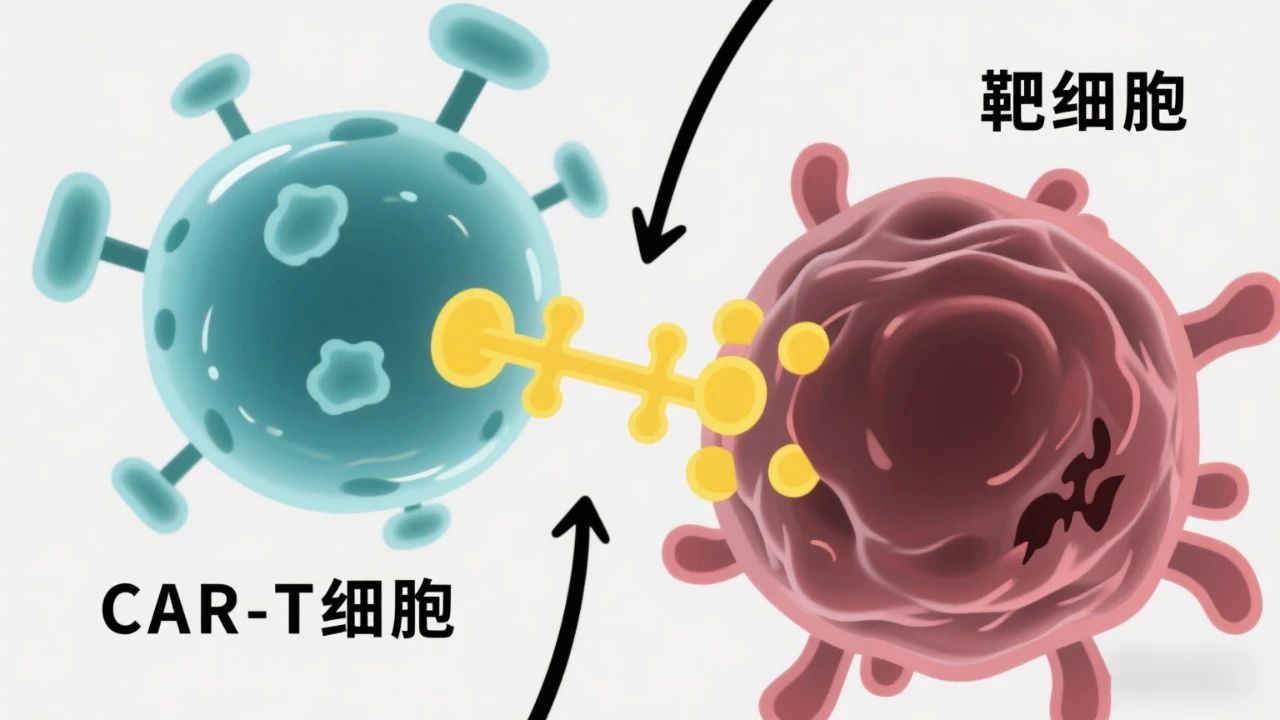
而CAR-T 外泌体,正是从经过基因改造的 CAR-T 细胞中提取的外泌体。它们继承了 CAR-T 细胞的 “抗癌武器”——表面携带识别癌细胞的嵌合抗原受体(CAR),同时具备外泌体的独特优势,成为精准打击癌细胞的 “纳米导弹”。
规避 “细胞因子风暴” 风险
CAR-T 细胞疗法最危险的副作用是细胞因子释放综合征(CRS)—— 大量活化的 CAR-T 细胞释放过量炎症因子,可能导致高热、低血压甚至器官衰竭。而CAR-T 外泌体的作为 “无细胞” 疗法,不会在体内增殖,也不会持续释放细胞因子,从根源上降低了 CRS 的发生风险。临床前研究显示,CAR-T 外泌体在发挥抗癌作用的同时,几乎不引发类似 CAR-T 细胞的全身炎症反应。
突破实体肿瘤 “壁垒”
实体肿瘤(如肺癌、乳腺癌、胰腺癌)之所以难治,在于其复杂的肿瘤微环境:致密的细胞外基质和低氧环境阻碍 CAR-T 细胞渗透以及肿瘤分泌抑制性分子(如 PD-L1),“阻碍” 免疫细胞发挥作用。
CAR-T 外泌体的优势在于:轻松穿越肿瘤基质,到达 CAR-T 细胞难以触及的深部癌细胞;不表达 T 细胞表面分子,不易被肿瘤微环境中的抑制信号干扰;可同时携带化疗药物(如紫杉醇)和免疫激活分子,实现 “化疗 + 免疫治疗” 双重攻击。
“现成疗法” 降低成本与门槛
CAR-T 细胞疗法是需要对每位患者进行“量身定制”,制备周期长(数周)、成本高昂(数十万美元)。而CAR-T 外泌体可通过标准化生产(如大规模培养 CAR-T 细胞后提取外泌体),制成 “通用型” 药物,大幅降低成本,缩短治疗周期。此外,外泌体稳定性高,便于储存和运输,更适合临床普及。
目前,CAR-T 外泌体已在多种癌症模型中展现潜力,部分研究已进入临床前阶段:
1. 血液肿瘤:延续 CAR-T 的辉煌
研究进展:在白血病、淋巴瘤模型中,CAR-T 外泌体通过表面 CAR 精准识别癌细胞(如 CD19 阳性细胞),释放穿孔素、颗粒酶等毒性分子,直接诱导癌细胞凋亡。与 CAR-T 细胞相比,其疗效相似,但 CRS 风险显著降低。
2. 实体肿瘤:攻克 “治疗盲区”
肺癌:靶向 EGFRvIII(肺癌常见抗原)的 CAR-T 外泌体,可穿透肿瘤组织,抑制肿瘤生长,联合紫杉醇加载的外泌体,能同时诱导癌细胞死亡和免疫激活。
乳腺癌:针对间皮素(MSLN)的 CAR-T 外泌体,在三阴性乳腺癌模型中显著缩小肿瘤,且无明显毒性。
胶质母细胞瘤:利用外泌体穿越血脑屏障的能力,靶向递送抗癌分子,为治疗胶质母细胞瘤提供了新思路。
尽管前景广阔,CAR-T 外泌体仍需突破以下瓶颈:
①规模化生产:目前外泌体提取依赖超速离心等复杂技术,需开发更高效的工业化生产工艺;
②靶向精准性:部分肿瘤抗原存在异质性(癌细胞表面抗原不一致),需优化 CAR 设计,实现更广谱的靶向;
③长期安全性:外泌体在体内的代谢路径、潜在蓄积风险仍需深入研究;
④临床转化:需开展更多动物实验和临床试验,验证其在人体中的疗效与安全性。
CAR-T 细胞疗法的诞生,标志着癌症治疗从 “化学药物” 迈向 “活细胞药物” 时代;而 CAR-T 外泌体的兴起,可能引领下一次革命 ——“无细胞免疫治疗”。这种“纳米级抗癌武器” 兼具精准性、安全性和灵活性,有望突破传统疗法的局限,为血液肿瘤和实体肿瘤患者带来新希望。
参考文献
Sani F, et al. CAR-T cell-derived exosomes: a new perspective for cancer therapy. Stem Cell Res Ther. 2024;15:174.
注:本文仅供科普参考,具体治疗方案请遵医嘱。

 0311-86576536
0311-86576536 新闻中心
新闻中心 风采展示
风采展示 信息公告
信息公告
 公众号
公众号 视频号
视频号

