非病毒CAR-T细胞疗法:癌症治疗的“无病毒”革命?
发布时间:2025-08-21

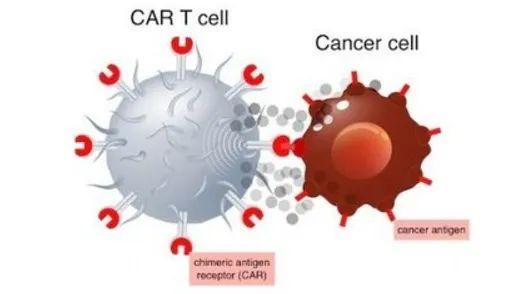
提起癌症治疗,近年来最令人振奋的突破之一莫过于CAR-T 细胞疗法。这种“活的药物” 通过提取患者体内的 T 细胞,经过基因改造后使其表达能识别癌细胞的嵌合抗原受体(CAR),再回输到体内,如同训练有素的 “细胞战士”,精准杀灭癌细胞。
截至 2025 年,全球已有多款病毒载体改造的 CAR-T 疗法获批,例如针对 CD19 阳性血液肿瘤的 Kymriah、Yescarta 等,在淋巴瘤、白血病等患者中实现了高达 80% 的完全缓解率。然而,这些疗法依赖病毒载体(如慢病毒、逆转录病毒)来完成基因改造,就像 “快递员” 一样将 CAR 基因送入 T 细胞,但病毒载体存在生产成本高、制备周期长(需 2-3 周)、潜在致癌风险等局限,如同带着 “枷锁” 的舞者,限制了其广泛应用。
为了突破病毒载体的瓶颈,科学家们将目光转向非病毒载体技术,试图用更安全、灵活的方式改造 T 细胞。目前主要有三大类技术路径:
转座子系统
转座子是基因组中的 “跳跃基因”,能将特定 DNA 片段插 入基因组,常见的包括 Sleeping Beauty(睡美人)和PiggyBac(猪尾巴)系统。
工作原理:
以 “睡美人” 为例,它由两部分组成:携带 CAR 基因的 “转座子 DNA” 和负责切割基因组的 “转座酶”。转座酶如同 “分子剪刀”,将 CAR 基因精准插入 T 细胞基因组,实现稳定表达,且避免了病毒载体的免疫原性问题。
优 势:
●成本低:生产流程简单,质粒成本仅为病毒载体的 1/5-1/10;
●灵活性高:可同时插入多个基因(如 CAR 和安全开关),适应未来 “多靶点 CAR-T” 的需求;
●安全性佳:“睡美人” 的整合位点接近随机,远离癌基因,而 “猪尾巴” 虽整合在转录活跃区域,但通过优化可降低风险。
临床进展:
美国 MD 安德森癌症中心利用 “睡美人” 系统开发的 CD19 CAR-T,在早期临床试验中使复发白血病患者获得长期缓解,且未出现严重毒性。欧洲的 CARAMBA 试验则使用 “睡美人” 联合 mRNA 转座酶,针对多发性骨髓瘤
mRNA技术
mRNA 技术因新冠疫苗而广为人知,在 CAR-T 领域同样展现潜力。
工作原理:
直接将编码 CAR 的 mRNA 通过电穿孔或纳米载体导入 T 细胞,mRNA 无需进入细胞核即可翻译出 CAR 蛋白,发挥作用后自然降解,避免基因组整合风险。
优 势:
●成本低:生产流程
●安全性极高:无插入突变风险,适合测试新靶点(如表达于健康组织的抗原);
●制备快速:从设计到生产仅需数天,可实现 “现货型” CAR-T 的快速制备。
挑 战:
CAR蛋白表达短暂(仅维持 2-4 次细胞分裂),可能影响疗效持久性。目前主要用于联合转座子系统,例如用 mRNA 递送转座酶,减少质粒用量和毒性。
纳米载体
纳米技术为基因递送提供了新工具,包括脂质纳米颗粒(LNP)、聚合物纳米载体等。
工作原理:
纳米颗粒如同 “飞船”,包裹 DNA 或 mRNA,通过靶向分子精准结合 T 细胞表面受体,将基因递送入细胞,避免电穿孔的细胞损伤。
创新应用:
●体内直接改造:无需体外培养 T 细胞,通过注射纳米载体在体内直接将 T 细胞转化为 CAR-T,简化流程;
●联合基因编辑:例如 CRISPR-Cas9 与纳米载体结合,实现 CAR 基因的定点插入,进一步提升安全性。
前 景:
美国 CoImmune 公司开发的纳米载体 CAR-T,已在动物模型中实现实体瘤的有效控制,且避免了传统方法的脱靶毒性。
非病毒 CAR-T 已从实验室走向临床,部分疗法展现出媲美甚至超越病毒载体的潜力:
血液肿瘤:
意大利团队利用 “睡美人” 系统开发的供体来源 CAR-T,在异基因造血干细胞移植后复发的白血病患者中,实现了 80% 的 CAR-T 细胞表达率,且无严重移植物抗宿主病(GvHD);
澳大利亚 CARTELL 试验使用 “猪尾巴” 系统的 CD19 CAR-T,在复发 B 细胞恶性肿瘤中响应率达 60%,但需警惕高拷贝数导致的潜在致癌风险(如 2 例 T 细胞淋巴瘤案例)。
实体肿瘤:
非病毒技术在实体瘤中面临更大挑战,如肿瘤微环境抑制 T 细胞功能。美国 PRGN-3007 疗法通过纳米载体递送多基因(CAR+IL-15+PD-1 阻断),在小鼠模型中显著增强 T 细胞持久性和抗肿瘤活性,目前已进入 Ⅰ 期临床试验。
非病毒技术的终极目标是实现低成本、高灵活、全通用的 CAR-T 疗法,主要方向包括:
1.多靶点 CAR-T:通过转座子系统同时插入多个 CAR 基因,识别肿瘤异质性抗原,例如同时靶向 CD19 和 CD22,减少抗原逃逸导致的复发;
2.现货型通用 CAR-T:利用健康供体 T 细胞结合非病毒改造,开发 “通用型” 产品,避免自体细胞制备的漫长等待;
3.体内直接给药:纳米载体介导的体内 CAR-T 生成,如同 “现场培训细胞战士”,无需体外培养,适合紧急治疗;
4.联合基因编辑:CRISPR-Cas9 敲除 T 细胞内源性 PD-1、TIM-3 等抑制性分子,再结合非病毒载体插入 CAR,双重增强疗效。
尽管前景光明,非病毒 CAR-T 仍面临技术瓶颈:
效率问题:部分非病毒方法(如 mRNA)的转染效率低于病毒载体,需优化递送系统;
长期安全性:转座子的随机整合虽风险较低,但仍需长期随访数据验证;
监管与生产:非病毒载体的规模化生产(如纳米颗粒的标准化制备)和质量控制仍是产业难点。
但正如 mRNA 疫苗在新冠疫情中的突破,技术迭代正在加速。或许在不久的将来,非病毒 CAR-T 将成为癌症治疗的主流选择,让更多患者受益于这场 “无病毒” 的医学革命。
从病毒载体到非病毒技术,CAR-T 疗法的进化史折射出医学领域对 “精准、安全、可及” 的永恒追求。非病毒 CAR-T 不仅是技术的革新,更是希望的传递 —— 它让我们看到,癌症治疗正从 “个体化定制” 迈向 “工业化生产”,从 “昂贵的救命药” 变为 “可负担的常规疗法”。
未来已至,让我们共同期待非病毒时代的癌症治疗新范式!
参考文献
[1] Moretti A, et al. The Past, Present, and Future of Non-Viral CAR-TCells. Frontiers in Immunology, 2022.
注:本文仅供科普参考,具体治疗方案请遵医嘱。

 0311-86576536
0311-86576536 新闻中心
新闻中心 风采展示
风采展示 信息公告
信息公告
 公众号
公众号 视频号
视频号

