免疫细胞治疗:癌症治疗史的新篇章
发布时间:2025-08-20

2025年4月17日,第26个世界肿瘤日如期而至。今年的主题聚焦“全程管理,全息发力”,呼吁从预防、诊断到治疗的全周期抗癌策略。在众多突破性进展中,免疫细胞治疗无疑是近年来最耀眼的明星。从“天价疗法”到逐步普惠,从血液瘤到实体瘤的攻坚,免疫细胞治疗正以惊人的速度重塑癌症治疗格局。
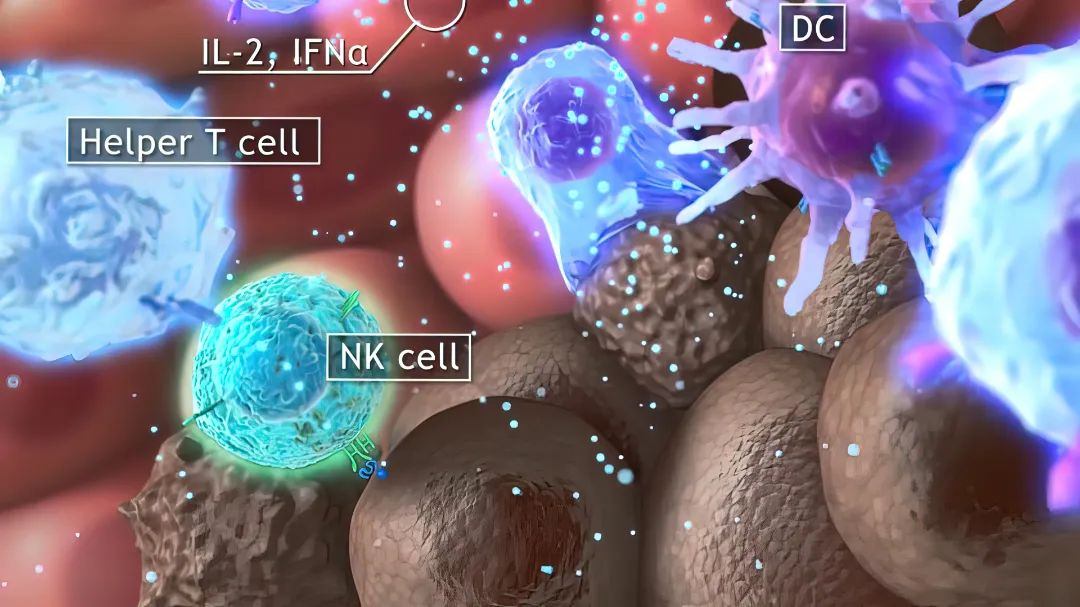
1、血液瘤:完全缓解率再创新高
2024年,全球首款无需风险评估策略(REMS)的CAR-T疗法Aucatzyl获批上市,用于复发/难治性B细胞急性淋巴细胞白血病(r/r B-ALL)。其Ib/II期临床数据显示,完全缓解率(CR)达57%,12个月无事件生存率(EFS)约50%。另一款靶向GPRC5D的CAR-T药物Arlo-Cel在治疗多发性骨髓瘤的1期试验中,总缓解率(ORR)高达87%,完全缓解率(CR)达53%,为晚期患者带来长期生存希望。
2. 实体瘤:胃癌、肝癌迎来新突破
中国研发团队针对CLDN18.2靶点的CT041疗法,在胃癌治疗中总应答率达48.6%,部分患者腹膜转移灶显著缩小。肝癌领域,靶向GPC3的CAR-T疗法在临床试验中显示晚期肿瘤显著缩小,为“癌中之王”提供了新武器。
2024年,美国FDA批准首款TIL疗法Lifileucel上市,用于晚期黑色素瘤。其全球II期试验数据显示,31.5%的患者肿瘤显著缩小甚至消失,部分患者持续缓解超过2年。在非小细胞肺癌(NSCLC)中,TIL疗法同样展现潜力:21.4%的客观缓解率(ORR)和79.2%的肿瘤负荷减少率,为经多线治疗失败的患者打开新窗口。
关键机制:TIL疗法通过提取患者肿瘤浸润淋巴细胞,体外扩增后回输,精准识别并攻击癌细胞。其优势在于无需基因改造,天然靶向肿瘤特异性抗原,尤其适用于突变负荷高的实体瘤。
NK细胞凭借“无需预激活、广谱杀伤”的特性,成为实体瘤免疫治疗的新焦点。2024年一项涵盖600例实体瘤患者的荟萃分析显示,NK细胞治疗的客观缓解率(ORR)为28.2%,疾病控制率(DCR)达63.2%。其中,肝细胞癌患者ORR高达72.3%,异体NK细胞疗效显著优于自体。
技术升级:通过基因编辑开发的CAR-NK疗法,可增强细胞穿透肿瘤微环境的能力。例如,靶向PD-L1的CAR-NK在临床试验中显示出持久的抗肿瘤活性,且细胞因子风暴风险低于CAR-T。
双抗药物通过同时靶向肿瘤抗原和免疫细胞,实现“精准激活+高效杀伤”。2025年,国产双抗迎来爆发:
- 依沃西单抗(PD-1/VEGF双抗):在非小细胞肺癌头对头试验中,无进展生存期(PFS)显著优于帕博利珠单抗(K药),成为首个单药击败K药的免疫药物。
- 卡度尼利单抗(PD-1/CTLA-4双抗):胃癌一线治疗中,总生存期(OS)较单纯化疗提升40%,且安全性更优。
未来趋势:三抗、四抗设计及双抗ADC(抗体偶联药物)正成为研发热点,旨在解决肿瘤异质性和耐药难题。
1. 新抗原疫苗:个体化精准狙击
BioNTech的mRNA新抗原疫苗BNT122,在胰腺导管腺癌(PDAC)的3年随访中,6例患者保持无病状态,中位无复发生存期(RFS)达13.4个月。其通过激活T细胞清除微转移灶,显著降低复发风险。
2. KRAS疫苗:打破“不可成药”魔咒
ELI-002疫苗靶向KRAS突变(常见于胰腺癌、结直肠癌),在I期试验中,6例患者达到完全缓解。其无需个体化设计,可快速制备,为“冷肿瘤”治疗提供新思路。
免疫检查点抑制剂+细胞疗法
IL-21联合PD-1抑制剂可重塑耗竭T细胞功能,显著提升抗肿瘤活性。临床前研究显示,IL-21工程化T细胞在肝癌模型中浸润能力增强,疗效持久。
局部治疗+系统免疫
钟鉴宏团队研究发现,新辅助TACE(肝动脉化疗栓塞)联合免疫+靶向治疗,可使中晚期肝癌患者总生存期提升30%,病理缓解率达67.3%。
从“谈癌色变”到“与癌共存”,免疫细胞治疗正将科幻变为现实。随着AI赋能药物设计、基因编辑技术迭代,未来十年或将见证更多“治愈”奇迹。正如2025全国肿瘤防治宣传周所倡导的——“全程管理,全息发力”,唯有科学、信念与人文关怀并重,方能在抗癌征途中赢得最终胜利。

 0311-86576536
0311-86576536 新闻中心
新闻中心 风采展示
风采展示 信息公告
信息公告
 公众号
公众号 视频号
视频号

